Forschungsprojekte
Die Gruppe Spine Biomechanics besteht aus Ingenieuren der ETH Zürich und Chirurgen der Universitätsklinik Balgrist. Gemeinsam betreiben sie translationale Forschung an der Schnittstelle zwischen biomechanischer Grundlagenforschung und der Entwicklung von klinischen Anwendungen. Der interdisziplinäre Ansatz garantiert ein hohes Maß an Expertise, um relevante klinische Fragestellungen zu untersuchen. Die Gruppe hat ein voll ausgestattetes Wirbelsäulenlabor mit maßgefertigten Versuchsaufbauten für biomechanische In-vitro-Experimente etabliert, welches dem Standard der weltweit führenden Biomechanik-Labore entspricht. Die Einrichtungen wurden für eine Vielzahl von biomechanischen Studien an menschlichen Wirbelsäulen-Kadavern genutzt, um die menschliche Anatomie und Gewebeeigenschaften zu untersuchen und zu charakterisieren. Die daraus gewonnenen Ergebnisse und Erkenntnisse fliessen in patientenspezifische, biomechanische Modelle ein, die zur Optimierung der präoperativen Operationsplanung genutzt werden.
Patientenspezifische FE-Modellierung in der Wirbelsäulenchirurgie
Der Fokus dieses Projekts liegt auf der Verbesserung der Behandlungsergebnisse von Wirbelsäulenoperationen durch die Finite-Elemente-basierte Funktionsanalyse und Operationsplanung.
Dieses Forschungsprojekt ist Teil des Hochschulmedizin Zürich Flagship-Projektes SURGENT (Surgeon Enhancing Technologies), welches als Kooperationsprogramm zwischen verschiedenen medizinischen und technischen Forschungseinrichtungen in Zürich entstanden ist. Das Ziel dieser Zusammenarbeit ist die Entwicklung und Nutzung modernster Technologien zur Verbesserung der Behandlung und der Patientensicherheit durch die Steigerung der chirurgischen Genauigkeit. Der Projektschwerpunkt liegt dabei in der Wirbelsäulenchirurgie und der Neurochirurgie.
In den letzten Jahrzehnten haben sich Computermodellierungsansätze als Instrumente für ein detaillierteres Verständnis der komplexen Mechanismen welche in der gesunden und der pathologischen Wirbelsäule auftreten, etabliert. Finite-Elemente-Modelle (FE-Modelle) ermöglichen die Berechnung von Belastungen in biologischen Geweben (z. B. Knochen, Bandscheiben, Nerven) sowie in den damit interagierenden Implantaten (z. B. Pedikelschrauben, Verbindungsstäbe, intervertebrale Cages). In diesem Projekt zielen wir darauf ab, mit Hilfe solcher Modelle eine funktionelle Analyse spezifischer Eingriffe durchzuführen und die möglichen Behandlungsoptionen durch eine quantitative Auswertung der Ergebnisse bei variierenden chirurgischen Parametern (z.B. Schraubenposition, Position und Krümmung der Verbindungsstäbe, Strategie zur Nervendekompression) zu bewerten. Mit automatisierten und effizienten biomechanischen Simulationen, welche individualisierte, aber dennoch niedrigkomplexe Modelle verwenden, möchten wir den Chirurgen relevante, quantitative Informationen liefer. Dies soll es dann ermöglichen, die Operationszeit zu reduzieren und die Genauigkeit bei der Umsetzung des Operationsplans zu erhöhen.
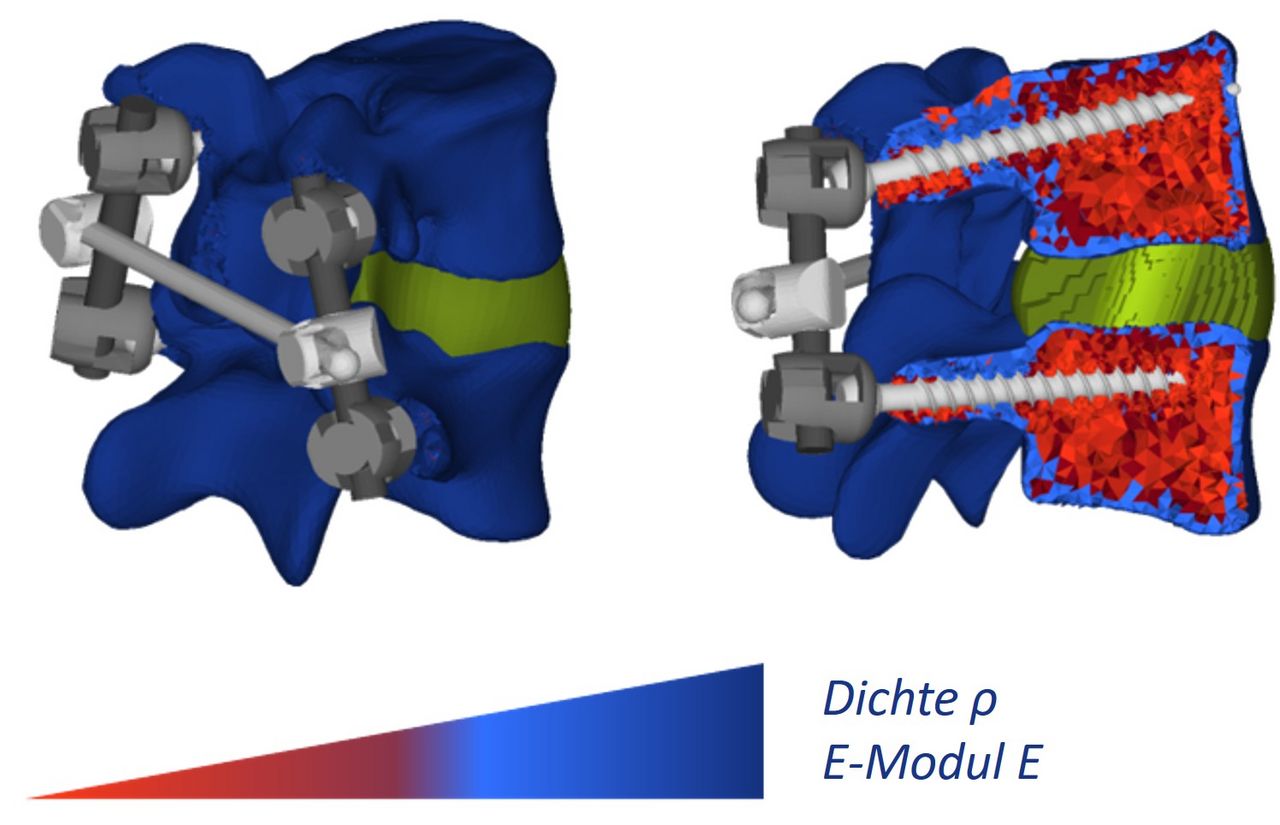
Abbildung 1: Finite-Elemente-Modell eines instrumentierten Lendenwirbelsäulensegments. Patientenspezifische Informationen werden in Form von Geometrie, Ausrichtung und Materialeigenschaften beim Modellerstellen berücksichtigt.
Für eine breite Anwendung eines solchen klinischen Arbeitsablaufes muss die Modellerstellung pazientenspezifisch und (halb-)automatisch erfolgen, denn die manuelle Modellierung einer großen Anzahl von Wirbelsäulen wäre eine mühsame und allgemein nicht praktikable Vorgehensweise. Als Ausgangspunkt verwenden wir anatomische Modelle, die basierend auf segmentierten Lendenwirbeln aus Computertomographie-Aufnahmen (CT-Aufnahmen) erstellt werden, auf welche dann ein wirbelspezifisches statistisches Formmodell (SSM) gefittet wird [1]. Die Korrespondenzeigenschaften der somit erhaltenen Netze ermöglichen es uns, Muskel- und Bandansatzpunkte, Randbedingungen, Facettengelenkflächen usw. für verschiedene Wirbelanatomien konsistent zu definieren. Ferner kann die individuelle Verteilung der Gewebeeigenschaften aus Bildern mit klinischer Auflösung gewonnen werden (Abbildung 1).
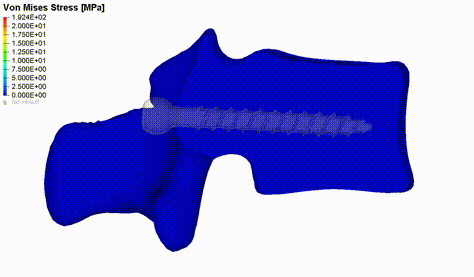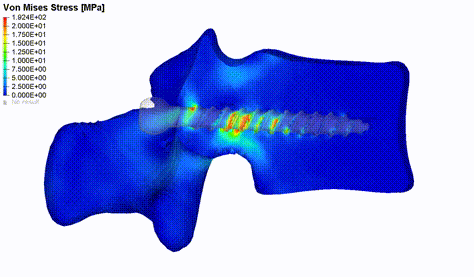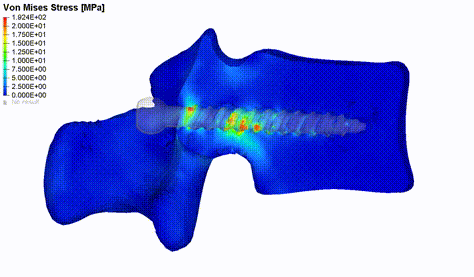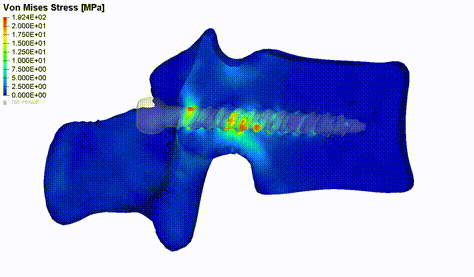
Abbildung 2: Verteilung der von Mises Spannung im Wirbelknochen während der Simulation eines Pedikelschrauben-Ausziehversuches.
Die Implementierung einer automatisierten Pipeline für die individualisierte biomechanische Modellierung kann bei der Untersuchung einer Vielzahl von klinischen Fragen helfen. Ein Problem, das es zu lösen gilt, ist zum Beispiel das Scheitern von Operationen aufgrund nicht optimaler Wechselwirkungen zwischen Gewebe und Implantat. Die Spondylodese ist ein etablierter chirurgischer Eingriff zur Verbesserung des Zustandes von Patienten mit Wirbelsäulenpathologien. Bei dieser Art der Operation werden eine oder mehrere Funktionseinheiten der Wirbelsäule dauerhaft miteinander versteift und eine häufige Komplikation im Zusammenhang mit diesem operativen Vorgehen ist die Schraubenlockerung. Wir haben ein FE-Ausziehmodell entwickelt und validiert, welches uns ermöglicht, die patientenspezifische Schraubenfixierung unter Einbeziehung der wirbeleigenen Knochendichteverteilung aus CT-Scans der Lendenwirbelsäule zu bewerten (Abbildung 2). Der primäre Output dieser Simulationen ist die Kraft, die erforderlich ist, um die Schraube aus dem Knochen zu ziehen, was ein Versagen an der Schnittstelle zwischen Schraube und Knochen anzeigt [2]. Das Modell wurde für eine erste Bewertung eines multikriteriellen genetischen Algorithmus verwendet, welcher darauf abzielt, die optimale Schraubenposition zu finden, indem die mechanischen Eigenschaften des Knochens in der Schraubenumgebung maximiert werden (Caprara et al., in Review). Die Modellierung des axialen Schraubenauszugs oder der kaudokranialen Belastung der Fusionsinstrumentierung kann ebenfalls helfen, den Hauptbelastungsmechanismus welcher die Schraubenlockerung verursacht, zu bestimmen. Hierfür können wir auf retrospektive Patientendaten zurückgreifen und Simulationsergebnisse zwischen Kohorten mit und ohne Schraubenlockerung in der Lendenwirbelsäule vergleichen.
Referenzen
- Caprara, S., Carrillo, F., Snedeker, J.G., Farshad, M., Senteler, M., 2021. Automated Pipeline to Generate Anatomically Accurate Patient-Specific Biomechanical Models of Healthy and Pathological FSUs. Front. Bioeng. Biotechnol. 9.
- Widmer, J., Fasser, M.-R., Croci, E., Spirig, J., Snedeker, J.G., Farshad, M., 2020. Individualized prediction of pedicle screw fixation strength with a finite element model. Computer Methods in Biomechanics and Biomedical Engineering 23, 155–167.




